Maßeinheit für den Wert bzw. den Maßstab (potentia Hydrogenii = Stärkekonzentration von Wasserstoff) für die Konzentration der aktiven Säuren in einer Lösung, der anhand der freien Wasserstoff-Ionen gemessen wird. Beim Weinbau ist dies ein wichtiges Kriterium für das Wachstum des Rebstocks, die Traubenreife sowie den Geschmack und die Haltbarkeit des Weines. Bereits der Gehalt im Boden (von alkalisch bis sauer) die Temperatur und die Niederschlagsmenge während des Vegetationszyklus sowie auch die Rebsorte hat bezüglich der Konzentration im Wein große Bedeutung. Es wird damit u. a. im Zusammenhang mit der Weinbereitung der Säuregrad (Azidität) im Boden und eines Weines ausgedrückt. Dies steht mit dem Säuregehalt im Wein (Summe verschiedener Säuren) zwar in Zusammenhang, sagt aber etwas völlig Anderes aus.
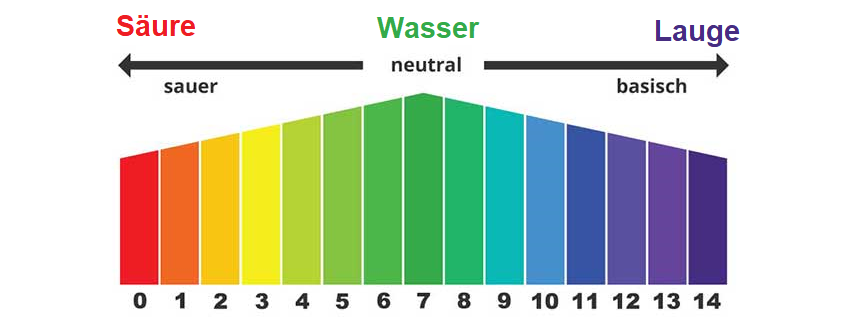
Säuregehalt (gr) und Säuregrad (pH)
Der Säuregehalt in Gramm per Liter oder in Promille besagt, welche Säuren in welcher Menge in einem Wein enthalten sind (siehe Tabelle unter Gesamtextrakt). Das hat noch nichts mit dem Säuregrad zu tun. Der Säuregrad in pH-Werten besagt, ob in Summe der Wein (oder irgendeine andere Lösung) sauer (0 bis 6,9 pH), neutral (7,0 pH = z. B. Wasser) oder alkalisch (7,1 bis 14 pH) ist. Je niedriger der Wert, desto höher ist der Säuregrad. Einen pH-Wert 0 besitzen zum Beispiel Schwefelsäure oder Salzsäure. Der pH-Wert für einen Wein beträgt im Durchschnitt zwischen 2,8 bis 3,8 pH. Er verändert sich übrigens im Laufe der Zeit während der Flaschenreifung bzw. Alterung des Weines nicht oder nur in geringfügigem Ausmaß.
Unterschied Säuregehalt und Säuregrad
Der pH-Wert besagt, ob ein Wein sauer, weniger sauer bis gar nicht sauer schmeckt. Dies ist nicht so sehr von dem durch Titration festgestellten Säuregehalt abhängig, sondern von der Menge, der Art und dem Wechselspiel der verschiedenen Säuren im Wein. Der Säuregehalt darf also nicht mit dem pH-Wert (Säuregrad) gleichgesetzt werden, da einige Stoffe im Wein alkalisch wirken und damit den Säuregrad abschwächen. Deshalb können zwei Weine mit gleichem Säuregehalt zwei verschiedene pH-Werte (das heißt Säuregrade) aufweisen. Dünne Weine mit niedrigem Gesamtextrakt haben neben einem hohen Säuregrad nur deshalb einen niedrigen pH-Wert, weil zu wenige Extraktstoffe vorhanden sind, die den Säuregrad abschwächen könnten.
Auswirkungen
Niedrige pH-Werte ergeben eine bessere Farbe, verhindern den Verderb durch Bakterien und erlauben mehr freies, aktives Schwefeldioxid. Beim Schwefeln gilt der Grundsatz: Je niedriger der pH-Wert, desto stärker ist die keimhemmende Wirkung und desto weniger Schwefel ist nötig. Eine malolaktische Gärung ist erst ab einem Wert von 3,2 pH aufwärts möglich. Bei zu hohen pH-Werten, wie sie in Weinen aus heißen Anbaugebieten oft vorkommen, können unerwünschte Bakterien den biologischen Säureabbau übernehmen. Sie können dann unangenehme Weinfehler wie Milchsäurestich und Pferdeschweiß verursachen.
weiterführende Informationen
Siehe eine Aufstellung aller Weininhaltsstoffe mit den durchschnittlichen Mengen unter dem Stichwort Gesamtextrakt. Bezüglich der Produktion von alkoholischen Getränken siehe unter Champagner (Schaumweine), Destillation (Destillate), Spezialweine, Spirituosen (Typen), Weinbereitung (Weine und Weintypen) und Weingesetz (weinrechtliche Belange).
Graphik: Wasserhelden
Stimmen unserer Mitglieder

Seriöse Quellen im Internet sind rar - und das Weinlexikon von wein.plus ist eine solche. Bei der Recherche für meine Artikel schlage ich regelmäßig im wein.plus-Lexikon nach. Dort erhalte ich zuverlässige und detaillierte Informationen.
Thomas Götz
Weinberater, Weinblogger und Journalist; Schwendi